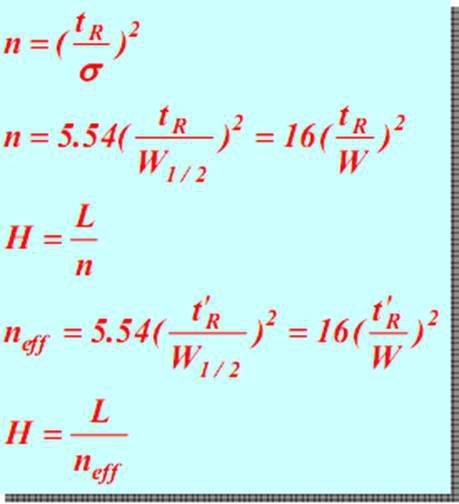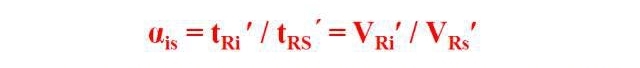kromatografi, juga dikenal sebagai "analisis kromatografi", "kromatografi", adalah metode pemisahan dan analisis, yang memiliki penerapan yang sangat luas dalam kimia analitik, kimia organik, biokimia, dan bidang lainnya.
Pendiri kromatografi adalah ahli botani Rusia M.Tsvetter.Pada tahun 1906, ahli botani Rusia Zvetter mempublikasikan hasil eksperimennya: Untuk memisahkan pigmen tumbuhan, ia menuangkan ekstrak petroleum eter yang mengandung pigmen tumbuhan ke dalam tabung kaca berisi bubuk kalsium karbonat dan mengelusinya dengan petroleum eter dari atas ke bawah.Karena pigmen yang berbeda mempunyai kapasitas adsorpsi yang berbeda pada permukaan partikel kalsium karbonat, dengan proses pencucian, pigmen yang berbeda bergerak ke bawah dengan kecepatan berbeda, sehingga membentuk pita dengan warna berbeda.Komponen pigmen dipisahkan.Dia menamakan metode pemisahan ini kromatografi.
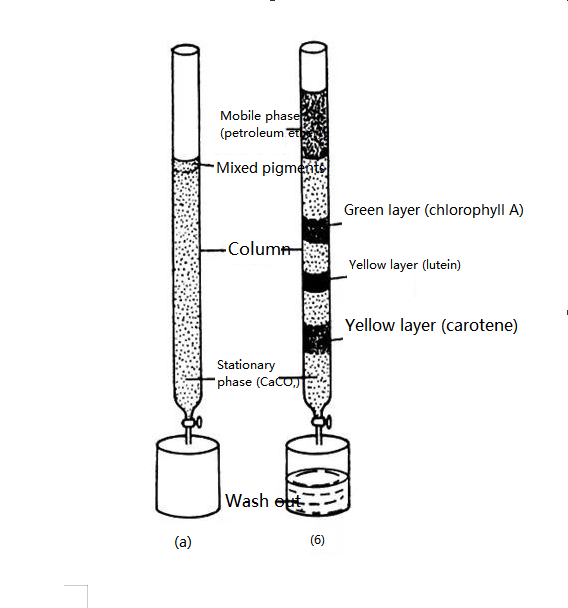
Representasi skema percobaan pemisahan pigmen daun tanaman
Dengan terus berkembangnya metode pemisahan, semakin banyak zat tak berwarna yang menjadi objek pemisahan, kromatografi juga secara bertahap kehilangan arti "warna", namun nama tersebut masih digunakan sampai sekarang.
Klasifikasi kromatografi
Inti dari kromatografi adalah suatu proses dimana molekul-molekul yang akan dipisahkan dipartisi dan diseimbangkan antara fase diam dan fase gerak.Zat yang berbeda dipartisi secara berbeda antara dua fase, yang menyebabkan zat tersebut bergerak dengan kecepatan berbeda dengan fase gerak.Dengan pergerakan fase gerak, berbagai komponen dalam campuran dipisahkan satu sama lain pada fase diam.Tergantung pada mekanismenya, ini dapat dibagi menjadi beberapa kategori.
1, menurut klasifikasi keadaan fisik dua fase
Fase gerak: Kromatografi gas, kromatografi cair, kromatografi fluida superkritis
Fase diam: gas-padat, gas-cair;Cair-padat, cair-cair
2, menurut bentuk klasifikasi fase diam
Kromatografi kolom: kromatografi kolom kemasan, kromatografi kolom kapiler, kromatografi kolom kemasan mikro, kromatografi preparatif
Kromatografi bidang: kromatografi kertas, kromatografi lapis tipis, kromatografi membran polimer
3, diklasifikasikan menurut mekanisme pemisahan
Kromatografi adsorpsi: Berbagai komponen dipisahkan menurut kapasitas adsorpsi dan desorpsinya pada adsorben
Kromatografi partisi: Berbagai komponen dipisahkan berdasarkan kelarutannya dalam pelarut
Kromatografi eksklusi molekul: sesuai dengan ukuran ukuran molekul pemisahan Kromatografi penukar ion: komponen afinitas yang berbeda untuk pemisahan resin penukar ion
Kromatografi afinitas: Pemisahan menggunakan adanya afinitas spesifik antara makromolekul biologis
Elektroforesis kapiler: komponen dipisahkan menurut perbedaan mobilitas dan/atau perilaku partisi
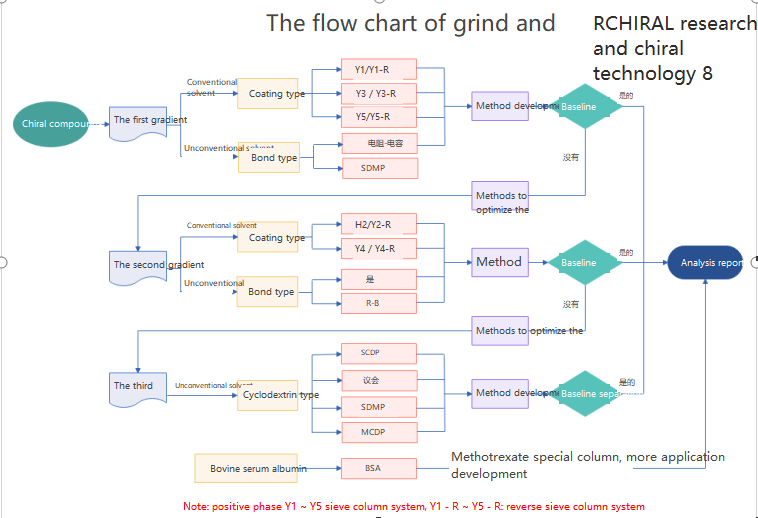
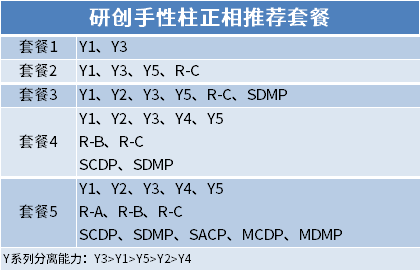
Kromatografi kiral digunakan untuk pemisahan dan analisis obat kiral, yang dapat dibagi menjadi tiga kategori: metode reagen derivatisasi kiral;Metode aditif fase gerak kiral;Metode resolusi fase diam kiral
Terminologi dasar kromatografi
Kurva yang diperoleh dengan memplot sinyal respons komponen setelah deteksi pemisahan kromatografi terhadap waktu disebut kromatogram.
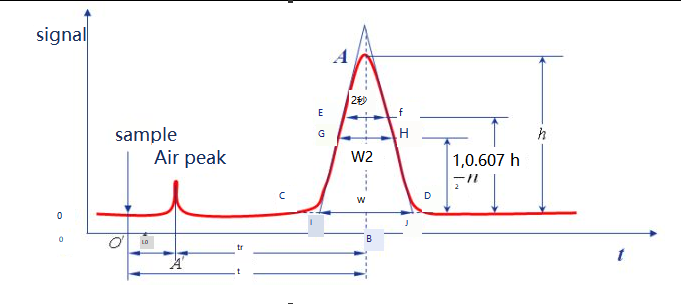
Dasar:Dalam kondisi kromatografi tertentu, kurva sinyal yang dihasilkan ketika hanya fase gerak yang melewati sistem detektor disebut garis dasar, seperti yang ditunjukkan pada garis ot.Bila kondisi percobaan stabil maka garis pangkalnya berupa garis yang sejajar sumbu mendatar.Garis dasar mencerminkan kebisingan instrumen, terutama detektor, seiring waktu.
Ketinggian puncak:jarak vertikal antara titik puncak kromatografi dan garis dasar, dilambangkan dengan h, seperti ditunjukkan pada garis AB'.
Lebar wilayah:Lebar wilayah puncak kromatografi berhubungan langsung dengan efisiensi pemisahan.Ada tiga metode untuk menggambarkan lebar puncak kromatografi: standar deviasi σ, lebar puncak W, dan FWHM W1/2.
Simpangan baku (σ) :σ adalah setengah jarak antara dua titik belok pada kurva distribusi normal, dan nilai σ menunjukkan derajat dispersi komponen menjauhi kolom.Semakin besar nilai σ, maka komponen efluen semakin tersebar dan efek pemisahannya semakin buruk.Sebaliknya, komponen efluen terkonsentrasi dan efek pemisahannya baik.
Lebar puncak W:Titik potong kedua sisi puncak kromatografi digunakan sebagai garis singgung, dan perpotongan pada garis dasar disebut lebar puncak, atau lebar garis dasar, yang juga dapat dinyatakan sebagai W, seperti ditunjukkan pada Gambar IJ.Berdasarkan prinsip distribusi normal, hubungan antara lebar puncak dan simpangan baku dapat dibuktikan W=4σ.
W1/2:Lebar puncak pada setengah tinggi puncak disebut FWHM, seperti yang ditunjukkan pada jarak GH.W1/2=2,355σ, W=1,699W1/2.
W1/2, W keduanya diturunkan dari σ dan digunakan untuk menghitung luas puncak selain mengukur efek kolom.Pengukuran FWHM lebih nyaman dan paling umum digunakan.
Ringkasan singkat
Dari kurva aliran puncak kromatografi, tujuan berikut dapat dicapai:
a, Analisis kualitatif dilakukan berdasarkan nilai retensi puncak kromatografi
b, analisis kuantitatif berdasarkan luas atau puncak puncak kromatografi
C. Efisiensi pemisahan kolom dievaluasi berdasarkan nilai retensi dan lebar puncak puncak kromatografi
Rumus perhitungan yang terlibat dalam kromatografi
1. Nilai retensi
Nilai retensi adalah parameter yang digunakan untuk menggambarkan sejauh mana suatu komponen sampel tertahan dalam kolom dan digunakan sebagai indikator karakterisasi kromatografi.Metode representasinya adalah sebagai berikut:
Waktu retensi tR
Waktu kematiantM
Sesuaikan waktu retensi tR'=tR-tM
(Total waktu yang dihabiskan dalam fase diam)
Volume retensi
VR=tR*F.(tidak bergantung pada kecepatan fase gerak)
Volume mati
VM=tM*Fc
(Ruang yang tidak ditempati oleh fasa diam pada jalur aliran dari injektor ke detektor)
Sesuaikan volume retensi VR'=t'R*Fc
2. Nilai retensi relatif
Nilai retensi relatif, juga dikenal sebagai faktor pemisahan, rasio koefisien partisi, atau faktor kapasitas relatif, adalah rasio waktu retensi (volume) yang disesuaikan dari komponen yang diuji dengan waktu retensi (volume) standar yang disesuaikan dalam kondisi kromatografi tertentu.

Nilai retensi relatif digunakan untuk menghilangkan pengaruh kondisi operasi tertentu, seperti laju aliran dan kehilangan fiksatif, terhadap nilai retensi.Standar dalam nilai retensi relatif dapat berupa komponen dalam sampel yang diuji atau senyawa yang ditambahkan secara buatan.
3. Indeks retensi
Indeks retensi adalah indeks retensi zat i yang akan diuji dalam larutan tetap X. Dua n-alan dipilih sebagai zat acuan, salah satunya memiliki nomor karbon N dan yang lainnya memiliki N+n.Waktu retensi yang disesuaikan masing-masing adalah t 'r (N) dan t 'r (N+n), sehingga waktu retensi yang disesuaikan t 'r (i) dari zat i yang akan diuji tepat berada di antara keduanya, yaitu, t 'r (N).
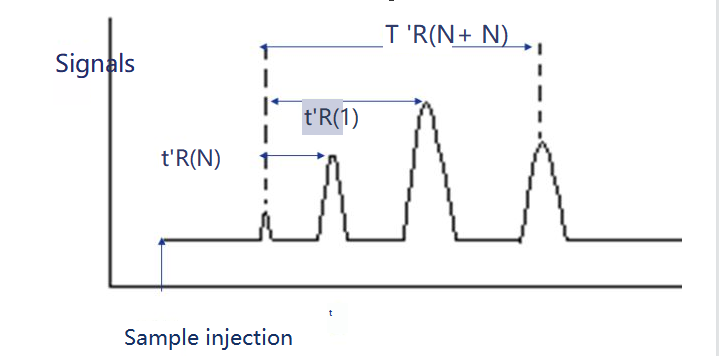
Indeks retensi dapat dihitung sebagai berikut.
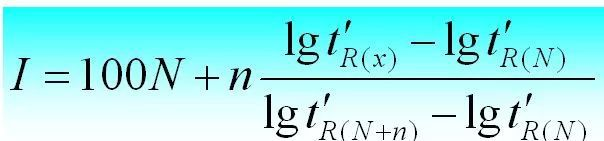
4. Faktor kapasitas (k)
Pada kesetimbangan, perbandingan massa suatu komponen dalam fasa diam (s) dengan fasa gerak (m), disebut faktor kapasitas.Rumusnya adalah sebagai berikut:
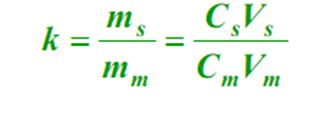
5、Koefisien partisi (K) Dalam kesetimbangan, perbandingan konsentrasi suatu komponen dalam fasa diam (s) dengan fasa gerak (m), disebut koefisien partisi.Rumusnya adalah sebagai berikut

Hubungan antara K dan k:
Ini mencerminkan tipe kolom dan simpulnya sifat-sifat penting struktur
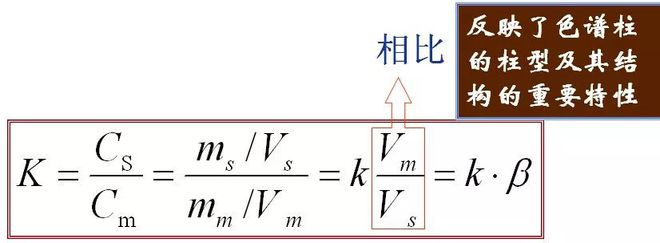
Ringkasan singkat
Hubungan antara nilai retensi dan faktor kapasitas dan koefisien partisi:
Pemisahan kromatografi didasarkan pada perbedaan kemampuan adsorpsi atau disolusi masing-masing komponen dalam sampel relatif tetap, yang secara kuantitatif dapat dinyatakan dengan besar kecilnya nilai koefisien partisi K (atau faktor kapasitas k).
Komponen dengan kemampuan adsorpsi atau disolusi yang kuat memiliki koefisien partisi (atau faktor kapasitas) yang besar dan waktu retensi yang lama.Sebaliknya, komponen dengan adsorpsi atau kelarutan yang lemah mempunyai koefisien partisi yang kecil dan waktu retensi yang singkat.
Teori dasar kromatografi
1. Teori baki
(1) Dikemukakan -- teori termodinamika
Ini dimulai dengan model pelat menara yang diusulkan oleh Martin dan Synge.
Kolom fraksinasi: dalam baki untuk beberapa kali kesetimbangan gas-cair, sesuai dengan titik didih pemisahan yang berbeda.
Kolom: Komponen diseimbangkan dengan beberapa partisi antara dua fase dan dipisahkan berdasarkan koefisien partisi yang berbeda.
(2) Hipotesis
(1) Terdapat banyak baki dalam kolom, dan komponen dapat dengan cepat mencapai kesetimbangan distribusi dalam interval baki (yaitu, ketinggian baki).
(2) Fase gerak memasuki kolom, tidak terus menerus tetapi berdenyut, yaitu setiap lintasan merupakan volume kolom.
(3) Ketika sampel ditambahkan ke setiap pelat kolom, difusi sampel sepanjang sumbu kolom dapat diabaikan.
(4) Koefisien partisi sama pada semua baki, tidak bergantung pada jumlah komponen.Artinya, koefisien partisi pada setiap taban adalah konstan.
(3) Prinsip
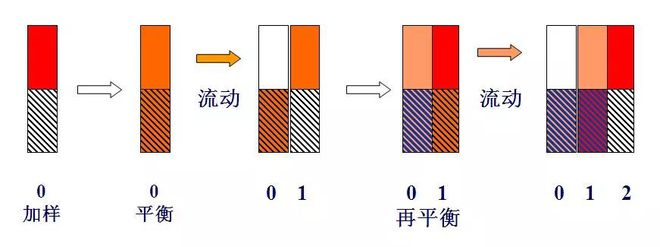
Diagram skema teori baki
Jika komponen satuan massa, yaitu m=1 (misalnya 1mg atau 1μg), ditambahkan ke baki No. 0, dan setelah kesetimbangan distribusi, karena k=1 yaitu ns=nm, nm=ns=0,5.
Ketika volume pelat (lΔV) gas pembawa memasuki pelat 0 dalam bentuk pulsasi, gas pembawa yang mengandung komponen nm dalam fasa gas didorong ke pelat 1. Pada saat ini, komponen ns dalam fasa cair pelat 0 dan komponen nm dalam fasa gas pelat 1 akan didistribusikan kembali antara dua fasa.Jadi, jumlah komponen yang terdapat pada pelat 0 adalah 0,5, fasa gas dan fasa cairnya masing-masing 0,25, dan jumlah total yang terdapat pada pelat 1 juga adalah 0,5.Fase gas dan cair juga 0,25.
Proses ini diulangi setiap kali gas pembawa volume pelat baru dimasukkan ke dalam kolom (lihat tabel di bawah).
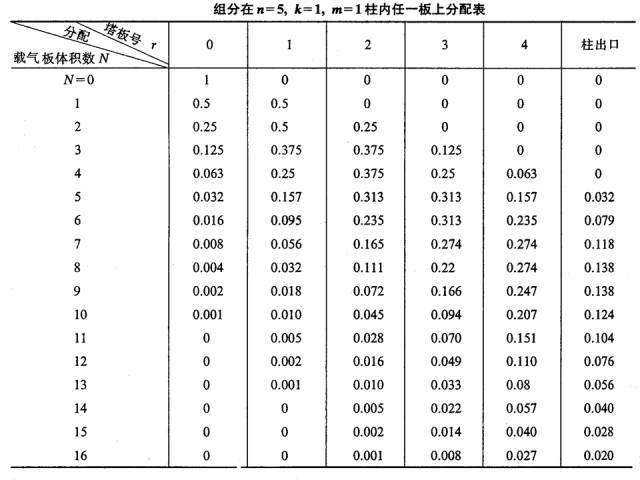
(4) Persamaan kurva aliran keluar kromatografi

σ adalah simpangan baku, adalah waktu retensi, C adalah konsentrasi setiap saat,
C, adalah konsentrasi injeksi, yaitu jumlah total komponen (area puncak A).
Pada konstanta tR, semakin kecil W atau w 1/2 (yaitu, semakin sempit puncaknya), semakin besar jumlah pelat teoritis n, semakin kecil tinggi pelat teoritis, dan semakin tinggi efisiensi pemisahan kolom.Hal yang sama juga berlaku pada teori efektif tray neff.Oleh karena itu, jumlah baki teoritis merupakan indeks untuk mengevaluasi efisiensi kolom.
(5) Ciri-ciri dan kekurangan
> Keuntungan
Teori baki bersifat semi empiris dan menjelaskan bentuk kurva aliran keluar
Proses partisi dan pemisahan komponen diilustrasikan
Sebuah indeks untuk mengevaluasi efisiensi kolom diusulkan
> Keterbatasan
Komponen-komponen tersebut tidak dapat benar-benar mencapai keseimbangan distribusi dalam dua fase:
Difusi longitudinal komponen dalam kolom tidak dapat diabaikan:
Pengaruh berbagai faktor kinetik terhadap proses perpindahan massa tidak dipertimbangkan.
Hubungan antara efek kolom dan kecepatan aliran fase gerak tidak dapat dijelaskan:
Tidak jelas faktor utama apa yang mempengaruhi efek kolom
Masalah-masalah ini diselesaikan secara memuaskan dalam teori laju.
2. Teori nilai
Pada tahun 1956, sarjana Belanda VanDeemter dkk.menyerap konsep teori baki, dan menggabungkan faktor kinetik yang mempengaruhi ketinggian baki, mengemukakan teori kinetik teori laju proses kromatografi, dan menurunkan persamaan VanDeemter.Ia menganggap proses kromatografi sebagai proses dinamis non-ekuilibrium dan mempelajari pengaruh faktor kinetik terhadap pelebaran puncak (yaitu efek kolom).
Kemudian, Giddings dan Snyder dkk.mengusulkan persamaan laju kromatografi cair (yaitu persamaan Giddings) berdasarkan persamaan VanDeemter (kemudian disebut persamaan laju kromatografi gas) dan menurut perbedaan sifat antara cairan dan gas.
(1) Persamaan Van Deemter
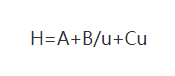
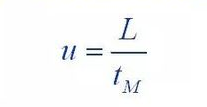
Dimana : H : adalah tinggi papan
A: koefisien istilah difusi pusaran air
B: koefisien istilah difusi molekul
C: koefisien suku hambatan perpindahan massa
(2) Persamaan Giddings
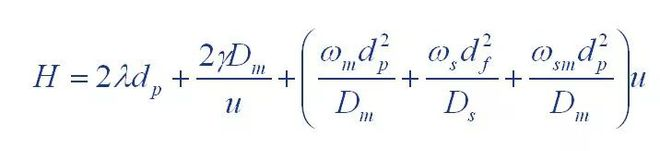
Analisis kuantitatif dan kualitatif
(1) Analisis kualitatif
Analisis kromatografi kualitatif bertujuan untuk mengetahui senyawa yang diwakili oleh setiap puncak kromatografi.Karena berbagai zat mempunyai nilai retensi tertentu pada kondisi kromatografi tertentu, nilai retensi dapat digunakan sebagai indeks kualitatif.Berbagai metode kualitatif kromatografi saat ini didasarkan pada nilai retensi.
Namun, zat yang berbeda mungkin memiliki nilai retensi yang serupa atau identik pada kondisi kromatografi yang sama, sehingga nilai retensi tidak eksklusif.Oleh karena itu sulit untuk mengkarakterisasi sampel yang sepenuhnya tidak diketahui berdasarkan nilai retensi saja.Jika berdasarkan pemahaman sumber, sifat dan tujuan sampel, penilaian awal terhadap komposisi sampel dapat dibuat, dan metode berikut dapat digunakan untuk menentukan senyawa yang diwakili oleh puncak kromatografi.
1. Pengendalian kualitatif dengan menggunakan bahan murni
Dalam kondisi kromatografi tertentu, suatu zat yang tidak diketahui hanya mempunyai waktu retensi tertentu.Oleh karena itu, zat yang tidak diketahui dapat diidentifikasi secara kualitatif dengan membandingkan waktu retensi zat murni yang diketahui pada kondisi kromatografi yang sama dengan waktu retensi zat yang tidak diketahui.Jika keduanya sama, zat yang tidak diketahui tersebut mungkin merupakan zat murni yang diketahui;Kalau tidak, maka yang tidak diketahui bukanlah substansi murni.
Metode pengendalian zat murni hanya dapat diterapkan pada zat yang belum diketahui komposisinya, komposisinya relatif sederhana, dan zat murninya telah diketahui.
2. Metode nilai retensi relatif
Nilai retensi relatif α, mengacu pada penyesuaian antara komponen i dan bahan referensi. Rasio nilai retensi:
Ini hanya berubah seiring dengan perubahan suhu fiksatif dan kolom, dan tidak ada hubungannya dengan kondisi pengoperasian lainnya.
Pada suhu fase diam dan kolom tertentu, nilai retensi yang disesuaikan dari komponen i dan zat referensi s diukur masing-masing, dan kemudian dihitung berdasarkan rumus di atas.Nilai retensi relatif yang diperoleh dapat dibandingkan secara kualitatif dengan nilai terkait dalam literatur.
3, menambahkan zat yang diketahui untuk meningkatkan metode ketinggian puncak
Jika terdapat banyak komponen dalam sampel yang tidak diketahui, puncak kromatografi yang diperoleh terlalu padat sehingga mudah diidentifikasi dengan metode di atas, atau jika sampel yang tidak diketahui hanya digunakan untuk analisis item tertentu.
“Pertama-tama dibuat kromatogram dari sampel yang tidak diketahui, dan kemudian kromatogram selanjutnya diperoleh dengan menambahkan zat yang diketahui ke sampel yang tidak diketahui.”Komponen dengan ketinggian puncak yang meningkat dapat diketahui zat tersebut.
4. Mempertahankan metode indeks kualitatif
Indeks retensi mewakili perilaku retensi zat pada bahan fiksatif dan saat ini merupakan indeks kualitatif yang paling banyak digunakan dan diakui secara internasional di GC.Ini memiliki keunggulan reproduktifitas yang baik, standar seragam dan koefisien suhu kecil.
Indeks retensi hanya berkaitan dengan sifat fasa diam dan suhu kolom, tetapi tidak dengan kondisi eksperimen lainnya.Akurasi dan reproduktifitasnya sangat baik.Selama suhu kolom sama dengan suhu fase diam, nilai literatur dapat diterapkan untuk identifikasi, dan tidak perlu menggunakan bahan murni untuk perbandingan.
(2) Analisis kuantitatif
Dasar kuantifikasi kromatografi:
Tugas analisis kuantitatif adalah menemukan ratusan komponen dalam sampel campuran
Konten pecahan.Kuantifikasi kromatografi didasarkan pada hal berikut: ketika kondisi operasi konsisten, adalah
Massa (atau konsentrasi) komponen yang diukur ditentukan oleh sinyal respon yang diberikan oleh detektor
Itu proporsional.Yaitu:
Dasar kuantifikasi kromatografi:
Tugas analisis kuantitatif adalah menemukan ratusan komponen dalam sampel campuran
Konten pecahan.Kuantifikasi kromatografi didasarkan pada hal berikut: ketika kondisi operasi konsisten, adalah
Massa (atau konsentrasi) komponen yang diukur ditentukan oleh sinyal respon yang diberikan oleh detektor
Itu proporsional.Yaitu:
1. Metode pengukuran luas puncak
Luas puncak adalah data kuantitatif dasar yang disediakan oleh kromatogram, dan keakuratan pengukuran luas puncak secara langsung mempengaruhi hasil kuantitatif.Metode pengukuran yang berbeda digunakan untuk puncak kromatografi dengan bentuk puncak yang berbeda.
Sulit untuk menemukan arti pasti musim dingin dalam analisis kuantitatif:
Di satu sisi karena sulitnya mengukur volume injeksi absolut secara akurat: di sisi lain
Area puncak bergantung pada kondisi kromatografi, dan strip kromatografi harus dipertahankan saat nilainya diukur
Tidaklah mungkin dan tidak nyaman untuk melakukan hal yang sama.Dan bahkan jika Anda bisa melakukannya dengan benar
Nilai pastinya, juga karena belum ada standar yang terpadu dan tidak bisa langsung diterapkan.
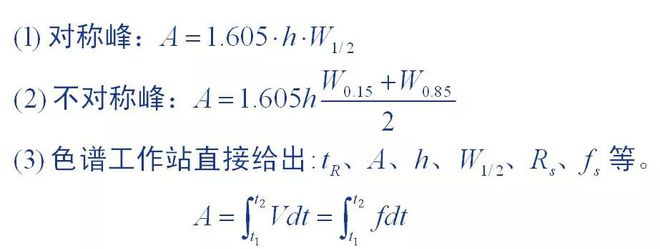
2. Faktor koreksi kuantitatif
Definisi faktor koreksi kuantitatif: jumlah komponen yang masuk ke detektor (m)
Perbandingan luas puncak kromatografi (A) atau tinggi puncak () merupakan konstanta proporsionalitas (,
Konstanta proporsionalitas disebut faktor koreksi absolut komponen.
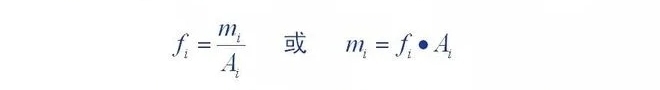
Sulit untuk menemukan arti pasti musim dingin dalam analisis kuantitatif:
Di satu sisi karena sulitnya mengukur volume injeksi absolut secara akurat: di sisi lain
Area puncak bergantung pada kondisi kromatografi, dan strip kromatografi harus dipertahankan saat nilainya diukur
Tidaklah mungkin dan tidak nyaman untuk melakukan hal yang sama.Dan bahkan jika Anda bisa melakukannya dengan benar
Nilai pastinya, juga karena belum ada standar yang terpadu dan tidak bisa langsung diterapkan.
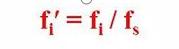
Artinya, faktor koreksi relatif suatu komponen adalah komponen dan bahan acuan s
Rasio faktor koreksi absolut.
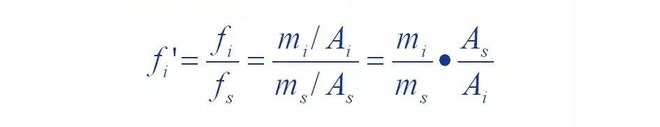
Terlihat bahwa faktor koreksi relatif adalah ketika kualitas komponen versus standar.
Jika zat s sama, maka luas puncak bahan acuan adalah luas puncak komponen
Banyak.Jika suatu komponen mempunyai massa m dan luas puncak A, maka bilangan f'A
Nilainya sama dengan luas puncak bahan acuan bermassa.Dengan kata lain,
Melalui faktor koreksi relatif, area puncak masing-masing komponen dapat dipisahkan
Dikonversi menjadi luas puncak bahan acuan sama dengan massanya, lalu perbandingannya
Standarnya terpadu.Jadi ini adalah metode yang dinormalisasi untuk mengetahui persentase setiap komponen
Dasar kuantitas.
Metode memperoleh faktor koreksi relatif: nilai faktor koreksi relatif hanya dibandingkan dengan yang ada
Pengukurannya terkait dengan standar dan jenis detektor, tetapi dengan strip operasi
Tidak masalah.Oleh karena itu, nilai-nilai dapat diambil dari referensi dalam literatur.Jika teks
Jika Anda tidak dapat menemukan nilai yang diinginkan dalam penawaran, Anda juga dapat menentukannya sendiri.Metode penentuan
Metode: Sejumlah zat terukur tertentu sepuluh bahan referensi terpilih → dibuat menjadi konsentrasi tertentu
Area puncak kromatografi A dan As dari kedua komponen diukur.
Itulah rumusnya.
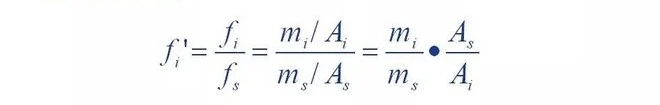
3. Metode perhitungan kuantitatif
(1) Metode normalisasi area
Jumlah isi semua fraksi bebas puncak dihitung sebagai 100% untuk kuantifikasi
Metode tersebut disebut normalisasi.Rumus perhitungannya adalah sebagai berikut:
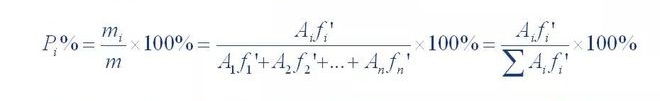
Dimana P,% adalah persentase kandungan komponen yang diuji;A1, A2... A n adalah komponen 1. Luas puncak 1~n;f'1, f'2... f'n adalah faktor koreksi relatif untuk komponen 1 sampai n.
(2) metode standar eksternal
Metode perbandingan kuantitatif antara sinyal respon komponen yang akan diuji dalam sampel dan komponen murni yang akan diuji sebagai kontrol.
(3) Metode standar internal
Yang disebut metode standar internal adalah suatu metode di mana sejumlah zat murni ditambahkan ke dalam larutan standar zat yang diuji dan larutan sampel sebagai standar internal, kemudian dianalisis dan ditentukan.
(3) metode penambahan standar
Metode penjumlahan standar, disebut juga metode penjumlahan internal, adalah dengan menambahkan sejumlah (△C)
Referensi zat uji ditambahkan ke dalam larutan sampel yang akan diuji, dan pengujian ditambahkan ke dalam pengujian
Puncak larutan sampel setelah zat lebih tinggi dibandingkan dengan larutan sampel asal
Pertambahan luas (△A) digunakan untuk menghitung konsentrasi zat dalam larutan sampel
Konten (Cx)
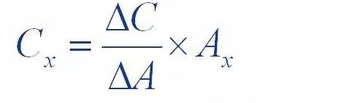
Dimana Ax adalah luas puncak zat yang akan diukur pada sampel asal.

Waktu posting: 27 Maret 2023